Alchimie
Transformez du cuivre en argent sans recours à la magie !
Réactifs
Sécurité
- Portez des gants et des lunettes de protection.
- Réalisez l’expérience sur le plateau en plastique.
- Portez des gants et des lunettes de protection.
- Réalisez l’expérience sur le plateau en plastique.
- Gardez un bol d’eau à proximité lorsque vous travaillez avec du feu.
- Enlevez les gants de protection avant d’allumer la baguette.
- Tenez les matériaux inflammables et les cheveux loin des flammes et de l'installation.
- N'éteignez pas le combustible solide. Laissez-le brûler complètement.
- Ne touchez pas le poêle après l’expérience. Attendez qu’il refroidisse.
- Éviter tout contact des produits chimiques avec les yeux ou la bouche.
- Éloigner les jeunes enfants, les animaux et les personnes sans équipement de protection des yeux de la zone où sont réalisées les expériences.
- Ranger ce coffret d’expériences hors de portée des enfants de moins de 10 ans.
- Nettoyer la totalité du matériel après utilisation.
- S’assurer que tous les récipients sont hermétiquement fermés et convenablement stockés après utilisation.
- S’assurer que tous les récipients vides sont correctement éliminés.
- Ne pas utiliser d’autre matériel que celui fourni avec le coffret ou recommandé dans la notice d’utilisation.
- Ne pas remettre les denrées alimentaires dans leur récipient d’origine. Les jeter immédiatement.
- En cas de contact avec les yeux : laver abondamment à l’eau en maintenant les yeux ouverts si nécessaire. Consulter immédiatement un médecin.
- En cas d’ingestion : rincer la bouche abondamment avec de l’eau, boire de l’eau fraîche. Ne pas faire vomir. Consulter immédiatement un médecin.
- En cas d’inhalation : transporter la personne à l’extérieur.
- En cas de contact avec la peau et de brûlures : laver abondamment à l’eau la zone touchée pendant au moins 10 minutes.
- En cas de doute, consulter un médecin sans délai. Emporter le produit chimique et son récipient.
- En cas de blessure, toujours consulter un médecin.
- L’utilisation incorrecte des produits chimiques peut engendrer des blessures et nuire à la santé. Réaliser uniquement les expériences décrites dans les instructions.
- Ce coffret d’expériences est à utiliser uniquement par des enfants de plus do 10 ans.
- Compte tenu de très grandes variations des capacités des enfants, même au sein d’un groupe d’âge, il convient que les adultes surveillants apprécient avec sagesse quelles sont les expériences appropriées et sans risque pour les enfants. Il convient que les instructions permettent aux adultes surveillants d’évaluer chacune des expériences afin de pouvoir déterminer son adéquation à un enfant particulier.
- Il convient que l’adulte surveillant s’entretienne des avertissements et des informations de sécurité avec l’enfant ou les enfants avant de commencer les expériences. Il convient d’accorder une attention particulière à la sécurité lors de la manipulation d’acides, d’alcalis et de liquides inflammables.
- Il convient que la zone où sont réalisées les expériences soit sans obstacle et ne soit pas située près d’une réserve de denrées alimentaires. Il convient qu’elle soit bien éclairée et aérée, et à proximité d’une adduction d’eau. Il convient d’utiliser une table solide dont la surface est résistante à la chaleur.
- Il convient d’utiliser complètement les substances contenues dans des emballages non refermables au cours d’une expérience, c’est-à-dire après l’ouverture de l’emballage.
FAQ et dépannage
Vous pensiez que les transformations « magiques » étaient terminées ? Loin de là !
Pour transformer un anneau d'« argent » ou d'« or » en cuivre, vous devez le plonger dans un acide (vous pourrez peut-être trouver de l'acide citrique dans votre cuisine). Comme vous vous en souvenez peut-être, le revêtement « argenté » de votre anneau n'est qu'une couche de zinc recouvrant le cuivre, et « l'or » n'est que du laiton, qui est une couche de particules de cuivre et de zinc mélangées. Les acides réagiront avec le zinc métallique qui passera à sa forme ionique, découvrant le cuivre intact. Ainsi, il ne restera que le cuivre pur sur la surface de l'anneau.
Et que faire pour transformer un anneau «doré » en anneau « argenté» ? Facile ! Essayez de l'enduire de zinc, en procédant comme vous l'avez fait au début de l'expérience. Ce revêtement devrait également bien adhérer au laiton !
Expérimentez toutes les options possibles : vous êtes désormais
« alchimiste : le maître de la pierre philosophale » !
Instructions pas à pas
Vous allez avoir besoin de beaucoup de chaleur pour cette expérience. Le combustible solide vous en fournit juste assez.

Versez une solution de sulfate de zinc ZnSO4 : elle contient des ions Zn2+. Le chlorure d'ammonium NH4Cl les aidera à se déplacer dans la solution et à interagir avec les autres participants de cette réaction.

Placez un anneau de cuivre Cu et un fil de zinc Zn dans le moule. Le Zn dont est composé le fil et le Zn2+ de la solution sont deux formes différentes du même élément : les particules de Zn sont recouvertes d'électrons tandis que les ions Zn2+ flottent librement dans la solution. Au lieu d'un anneau de cuivre, vous pouvez utiliser une pièce en cuivre. Assurez-vous simplement de bien la nettoyer auparavant.

L'anneau en cuivre devient argenté sous vos yeux !

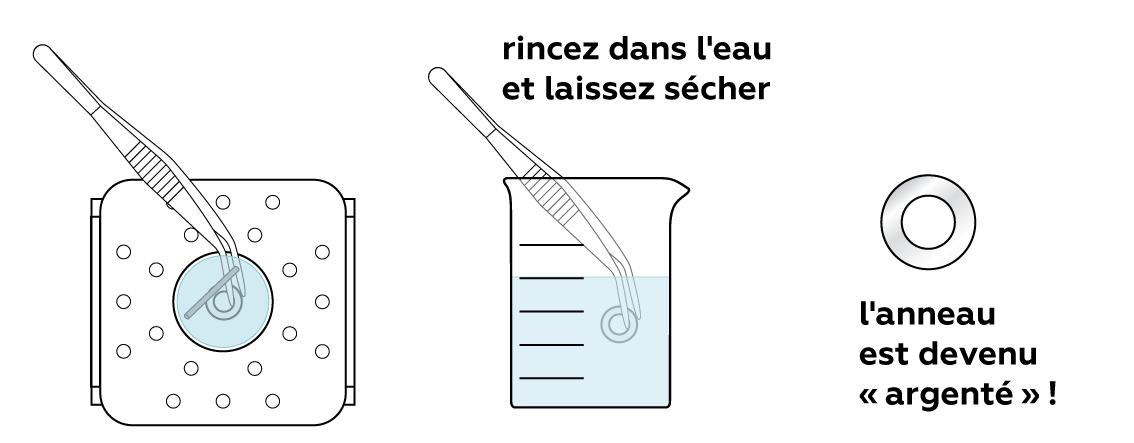
Pour rendre l'anneau encore plus chic, rincez-le sous l'eau. Mais avez-vous vraiment réussi à transformer du cuivre en argent ?
Élimination des déchets
Veuillez vous reporter aux réglementations locales pour la collecte des déchets chimiques. Jetez les autres déchets solides avec les ordures ménagères. Versez les solutions restantes dans l'évier. Rincez abondamment à l’eau.
Description scientifique





existent sous forme de particules chargées positivement (





et vice-versa
. Mais parfois, elles se déposent sur le cuivre
au lieu du zinc, car leurs nuages d'électrons sont trop proches les uns des autres. C'est ainsi que l'anneau de cuivre se recouvre d'une couche de zinc
qui ressemble à de l'argent.


Bien qu'il soit impossible de transformer un élément en un autre par réarrangement d'atomes, la science peut aujourd'hui changer les atomes eux-mêmes ! Les physiciens nucléaires transforment aisément un élément en un autre. Mais c'est une toute autre histoire…
Ça, c’est intéressant !
Comment pouvons-nous réellement transformer quelque chose en or ?
La chimie étudie le réarrangement des atomes, et non les transformations des atomes eux-mêmes. Elle est donc impuissante lorsqu'il s'agit d'obtenir de l'or à partir d'autres éléments. C'est une tâche pour la physique nucléaire ! Dans un réacteur nucléaire, certains éléments sont convertis en d'autres ; par exemple, l'uranium peut être transformé en plutonium et le soufre en chlore. Fabriquer de l'or artificiel est aussi possible... Mais cela en vaut-il la peine ?
Le moyen le plus abordable pour fabriquer de l'or artificiel est la désintégration radioactive de ses voisins du tableau périodique : le mercure et le platine. La transformation du platine en or n'est pas du tout rentable, car le premier est plus cher. Et même si le mercure est moins cher, le processus de transformation est, lui, extrêmement coûteux et laborieux. De plus, seulement une petite quantité du « métal noble » peut être obtenue de cette façon. De ce fait, l'exploitation de l'or par des réacteurs nucléaires est possible, mais n'est pas viable à l'heure actuelle, puisque le processus de fabrication de l'or par réactions nucléaires est plus onéreux que l'or lui-même.
Par tradition, les médailles d'or sont décernées pour la première marche du podium, l'argent pour la deuxième et le bronze pour la troisième. Pourquoi ?
Tout d'abord, le bronze est un alliage composé d'environ 80 % de cuivre et 20 % d'étain. Il suffit de jetter un œil sur le tableau périodique pour voir que le cuivre Cu, l'argent Ag et l'or Au sont tous situés dans la même colonne. Le tableau périodique est organisé de telle manière que les éléments d'une même colonne ont tendance à avoir des propriétés similaires. Ainsi, les métaux « olympiques » ont ceci en commun, qu'on les trouve à l'état pur dans la nature. Et ce, à la différence d'autres métaux, qui ne se trouvent généralement dans la nature que sous forme de composés complexes. Ces métaux ont également la particularité d'être assez malléables, ce qui les rend adaptés à la production d'articles tels que les médailles olympiques.
Mais les propriétés qu'ils ont en commun ne sont pas la seule chose que le tableau périodique nous révèle sur ces métaux. Les éléments sont classés dans le tableau périodique par ordre croissant de masse. Ceux qui ont la plus faible masse sont les plus abondants dans la nature. Le cuivre étant le plus léger des trois, nous pouvons conclure qu'il est beaucoup plus répandu dans la croûte terrestre. L'argent, situé un rang en dessous dans le tableau périodique, est un peu moins courant, et l'or, qui a le numéro atomique le plus élevé de ces trois métaux précieux, en est par conséquent le plus rare.
Ainsi, l'ordre des médailles, dont l'importance augmente du bronze, à l'argent, à l'or, est basé sur la rareté de ces éléments, tandis que le choix d'utiliser ces matériaux pour fabriquer des médailles repose sur leurs propriétés physiques.
Cependant, les médailles d'or olympiques actuelles sont, en réalité, constituées essentiellement d'argent. La couleur or provient des 6 grammes d'or pur qui sont utilisés pour dorer l'extérieur, représentant à peine un peu plus de 1% du volume total de la médaille.